近日,我校癌症研究院周哲敏教授联合詹启敏院士团队,在国际顶尖微生物学术期刊《细胞宿主与微生物》Cell Host & Microbe在线发表了题为“Strain-Level Genetic Heterogeneity and Colonization Dynamics Drive Microbiome Therapeutic Efficacy”的研究论文。该研究不仅在临床试验中提示了粪菌移植(FMT)联合免疫治疗可显著改善PD-L1阴性非小细胞肺癌患者的预后,更通过跨疾病队列的大规模数据分析,揭示了肠道微生物在定植动力学与种内遗传异质性方面的普适性规律。这一成果为下一代精准微生态药物的设计与定植干预提供了关键的理论框架。

研究团队首先针对晚期PD-L1阴性非小细胞肺癌免疫治疗敏感度低这一临床难点,开展了前瞻性临床试验,结果显示FMT联合抗PD-1治疗将患者的一年无进展生存期(PFS)从传统治疗的28%提升至55%。为了破解疗效背后的微生态密码,团队开发了基于480个超保守单拷贝基因的高分辨率菌株追踪框架ucgMLST。通过对肺癌、黑色素瘤、肠易激综合征及艰难梭菌感染等涵盖2000余份样本的8个跨疾病队列分析,研究发现传统物种水平的丰度分析难以解释疗效差异,更多功能差异隐藏在菌株水平的遗传异质性中。例如,Faecalibacterium duncaniae等物种在不同进化分支上展现出截然相反的临床效应,健康相关菌株富含增强肠道屏障的功能基因,而疾病相关菌株则富集应激适应相关基因。
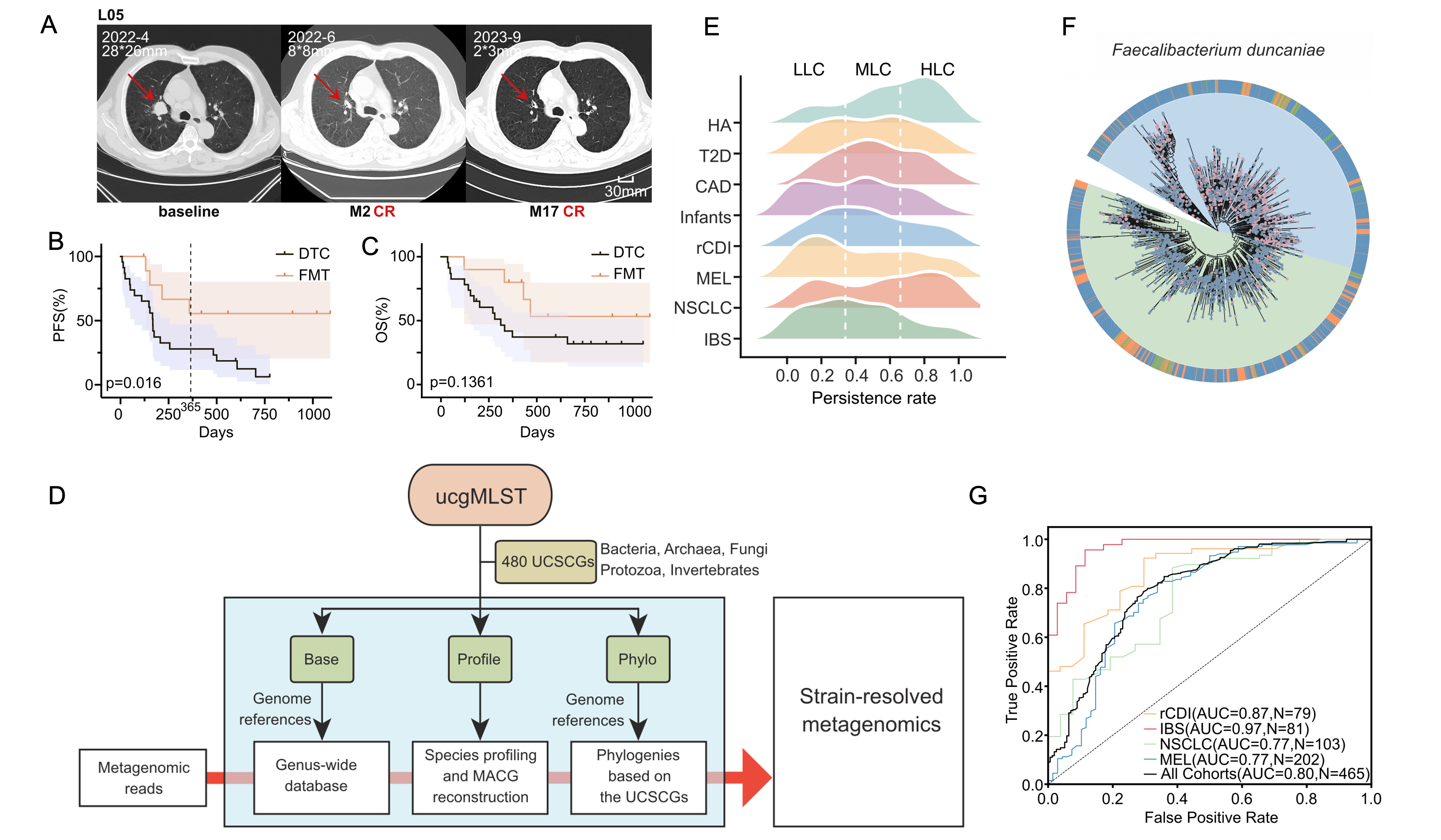
为了将这些生态规律转化为临床应用,研究团队开发了健康菌株评分(HSIM)系统,用于量化个体微生态的健康程度。该评分在多个独立验证队列中展现出强大的鲁棒性,能够跨疾病预测治疗反应并辅助供体筛选。基于定植潜力和临床获益的综合评估,研究进一步锁定了38种具有高定植潜能且功能确证的“优先物种”,为构建标准化、可精准递送的合成菌群药物提供了核心候选库。
苏州大学附属第一医院肿瘤科陈凯教授、刘伊娜、荣洁、苏州市疾病预防控制中心戴宁彬及苏州大学附属第一医院肿瘤科徐彩华博士为该论文共同第一作者;苏州大学周哲敏教授、詹启敏院士、夏淑婷副研究员及徐鉴城副研究员为该论文共同通讯作者。该研究得到了国家自然科学基金、国家生物药技术创新中心人才项目、江苏省自然科学基金、苏州市顶尖人才团队项目等多项资金的资助支持。苏州市健康医疗数智创新实验室为该研究提供了真实世界数据支持。该研究的发表标志着苏州大学癌症研究院在人体微生态与精准肿瘤治疗的交叉研究领域取得了重要突破,为推动微生态疗法从“粗放移植”向“精准干预”跨越提供了理论和数据基础。
文章链接:
https://www.sciencedirect.com/science/article/pii/S193131282600048X








