11月4日,国际权威期刊《 Nature Reviews Drug Discovery》(影响因子47.12)上在线发表了我校转化医学研究院院长、苏州大学附属第一医院副院长时玉舫教授与中国科学院健康科学研究所王莹研究员及博士研究生杜黎明和林良宇共同撰写的题为“Tumour-associated Mesenchymal Stem/Stromal Cells: Emerging Therapeutic Targets”特邀综述文章。
时玉舫教授领衔的团队结合自身在间充质干细胞(mesenchymal stem/stromal cells, MSCs)与肿瘤微环境方面多年的研究实践,系统地总结了肿瘤相关间充质干细胞(Tumour-associated mesenchymal stem/stromal cells, TA-MSCs)的特性,及其在肿瘤免疫微环境塑造、肿瘤生长与转移、化疗抵抗和免疫治疗中的作用及机制,为靶向性调控TA-MSCs,进而有效控制和治疗肿瘤提供了新的策略和方向。同时,利用MSCs在多种炎症损伤性疾病治疗中的临床应用潜能,并基于其载体功能和免疫调节可塑性,提出了MSCs在肿瘤靶向治疗中的应用新方向。
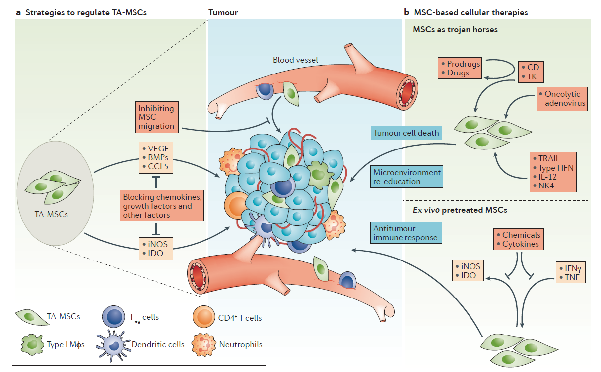
MSCs是一类广泛存在于机体各个组织器官的具有多种分化潜能的干细胞,对于维持组织内稳态具有不可忽视的作用。通过感知损伤信号,MSCs可以被招募至损伤部位,以“细胞代替”和“细胞赋能”方式,调控损伤部位的免疫微环境,促进组织修复。肿瘤作为“永不愈合的创伤”,能够通过分泌趋化因子和生长因子等信号招募MSCs至肿瘤微环境,并将其“驯化”成具有促肿瘤能力的TA-MSCs,为肿瘤的发生发展提供了肥沃的“土壤”。TA-MSCs与肿瘤细胞、免疫细胞之间的“a Menage-a-Trois(三角调控)”决定了TA-MSCs对肿瘤微环境的塑造和肿瘤细胞的调控,影响肿瘤的生长及转移,乃至放化疗的反应性。1)TA-MSCs调控T细胞、巨噬细胞、中性粒细胞等多种免疫细胞,促进肿瘤免疫微环境的形成,帮助肿瘤细胞逃逸免疫细胞的杀伤作用;2)TA-MSCs通过高表达多种生长因子,直接促进肿瘤细胞增殖;3)TA-MSCs可以招募内皮细胞的前体细胞以及分泌促血管生成因子,促进肿瘤组织的血管生成,为肿瘤生长提供丰富的营养;4)TA-MSCs表达多种趋化因子、细胞外基质蛋白等,构建肿瘤的“前转移”环境,促进了肿瘤细胞的远端转移;5)TA-MSCs能够帮助肿瘤细胞抵抗放疗、化疗和免疫疗法等多种治疗手段。鉴于TA-MSCs在肿瘤病理进程中的重要性,时玉舫教授的团队总结了靶向TA-MSCs及其调控肿瘤发生和发展的关键因子在肿瘤治疗中的应用潜能。同时,从MSCs临床应用潜能出发,结合该细胞的肿瘤趋化性和免疫调节作用的可塑性,提出MSCs在肿瘤靶向治疗中的“特洛伊木马”新策略,并将其分类为Assassination、Deployment、Contra suppression等不同抗肿瘤方式。至此,该综述基于对TA-MSCs在肿瘤病理进程中作用机制的系统认识,针对性提出靶向调节TA-MSCs的上下游调控信号分子在肿瘤治疗中的应用潜能,以及MSCs作为载体携带抗肿瘤药物杀伤肿瘤细胞和重塑抗肿瘤免疫微环境的应用前景,为理解TA-MSCs的功能和发现抗肿瘤新策略提供了方向。
文章链接:http://www.nature.com/nrd/journal/vaop/ncurrent/full/nrd.2016.193.html